 |
 |
|
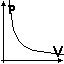
Il lavoro e' uguale all'area sottesa dalla linea che rappresenta la trasformazione. |
W= ∫pdV = NkT∫dV/V = NkT logV integrale indefinito
W = NkT logV2 - NkT logV1 sostituito limiti di integrazione
= NkT log(V2/V1)
U=N(3/2)kT per gas monoatomico
U e' funzione solo della temperatura, quindi Tk ⇒ Uk ∆U=0
Q=W
Non ha senso il calore specifico a T costante, poiche' per aver senso la sua definizione, la T deve variare. Un altro modo di vederla e' che e' infinito, dato che e' assorbe calore senza aumentare T.
Studio dei casi di dipendenza nell'eq di stato dei gas perfetti.
Possiamo pensare che siano entrambi effetti della velocita' delle particelle.
come e' possibile "Ricevere calore senza aumentare di temperatura" ?
poiche' il riscaldamento dell'acqua e' il fenomeno a cui siamo piu' abituati: se si fornisce calore all'acqua, allora aumenta di T, precisamente seguendo la legge Q=mc∆T.
Come e' possibile ? R: un gas espandendosi diminuisce di temperatura ! diminuzione che puo' essere usata per compensare l'aumento dovuto all'assorbimento di calore; se fatto contemporaneamente, in totale la T e' costante.
Dilatazione dell'acqua e dell'aria a confronto.
Processo isotermo
| partendo da uno stato di equilibrio:
cedo calore al corpo, una piccola quantita', al limite infinitesima, si crea un leggero disequilibrio: ⇒ la pressione esterna diminuisce ⇒ la pressione interna supera la pressione esterna ⇒ la differenza di pressione crea una forza risultante ⇒ la forza risultante mette in moto l'espansione ⇒ l'espansione fa lavoro ⇒ lavoro a spese dell'en interna che diminuisce ⇒ T diminuisce ⇒ p diminuisce, ⇒ p interna = p esterna ⇒ forza risultante = 0 |
|
biforcazione nel proseguire |
|
nuovo stato di equilibriocedo calore al corpo per aumentare la T al valore iniziale, tengo il volume costante. Il nuovo stato di equilibrio e' diverso dal precedente, poiche' il volume e' aumentato, non so p da questo ragionamento. |
l'espansione procedela sequenza di trasfrmazione si ripete: nuovo calore entra nel corpo, il leggero disequilibrio e' mantenuto ⇒ l'espansione procede
|